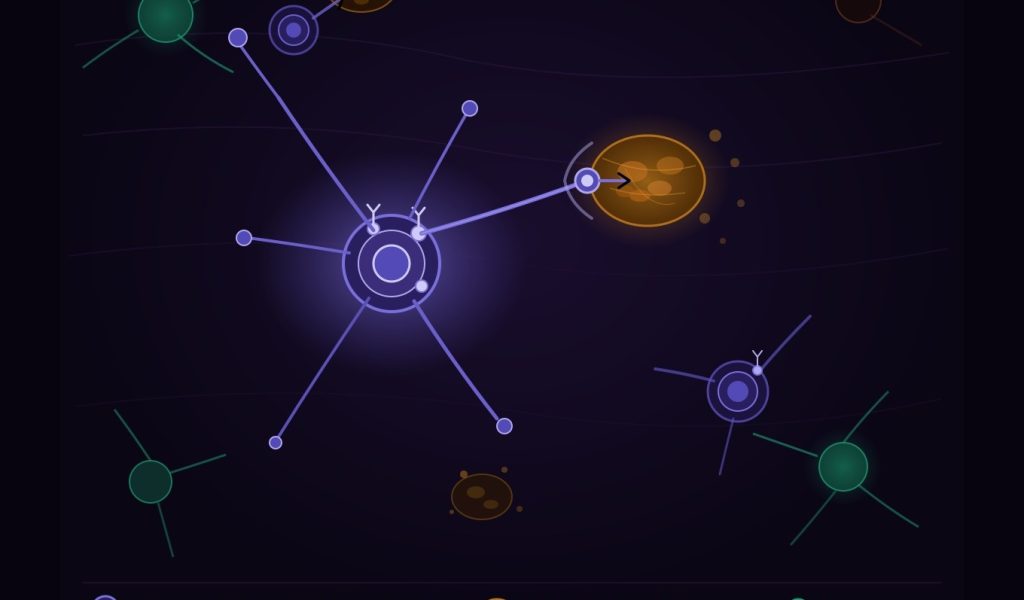
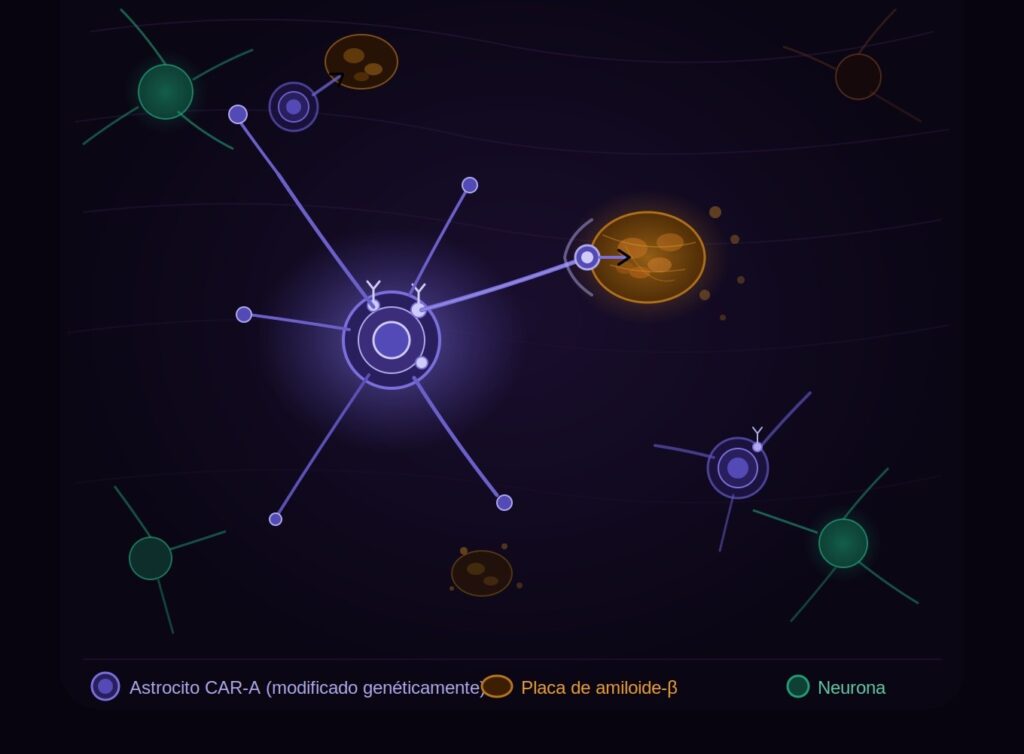
Las inmunoterapias dirigidas al péptido beta-amiloide (Aβ) son prometedoras para el tratamiento de la enfermedad de Alzheimer. Chen et al . desarrollaron una estrategia anti-Aβ basada en un sistema de receptor de antígeno quimérico (CAR) denominado CAR-A, en el que los astrocitos se modifican genéticamente mediante virus adenoasociados para expresar fragmentos variables de cadena simple de anticuerpos anti-Aβ conjugados a los dominios intracelulares de los receptores fagocíticos (véase la Perspectiva de Boles y Gate). Las pruebas in vitro y en ratones demostraron la eficacia de CAR-A para reducir la formación de placas de Aβ mediante la actividad coordinada de astrocitos y microglía. Estos resultados sugieren que CAR-A podría ser eficaz para reducir la progresión de la enfermedad de Alzheimer. —Mattia Maroso.
La enfermedad de Alzheimer (EA) es la causa más común de demencia relacionada con la edad en todo el mundo. Su patología progresa desde la acumulación de beta-amiloide (Aβ) extracelular hasta el desarrollo de tauopatía intraneuronal, lo que finalmente resulta en neurodegeneración. Actualmente, la estrategia más eficaz para ralentizar la progresión de la EA consiste en anticuerpos monoclonales anti-Aβ, tres de los cuales han recibido recientemente aprobación clínica. Sin embargo, estas terapias comparten varias limitaciones, como la necesidad de dosis altas y administración repetida, un estrecho margen terapéutico, riesgos como anomalías en las imágenes relacionadas con el amiloide y la dependencia de la señalización de la subunidad gamma del receptor Fc (FcRγ). Estos desafíos ponen de manifiesto la necesidad de nuevos enfoques terapéuticos.
RAZÓN FUNDAMENTAL
Los receptores de antígenos quiméricos (CAR) se pueden diseñar fusionando un fragmento variable de cadena simple (scFv) anti-Aβ al dominio intracelular de receptores fagocíticos seleccionados, creando un sistema autosostenible que permite a la glía cerebral reconocer y eliminar los agregados de Aβ. Este enfoque evita la administración repetida de dosis y permite ajustar con precisión la señalización intracelular, una capacidad que no ofrecen las terapias con anticuerpos convencionales. Dado que reemplazar la microglía endógena con células mieloides que expresan CAR sigue siendo un desafío para lograr una cobertura cerebral duradera, optamos por una población glial fagocítica alternativa: los astrocitos. Por lo tanto, generamos astrocitos que expresan CAR (CAR-A) y probamos su capacidad para eliminar la patología amiloide en un modelo de ratón con placas amiloides mediante la administración sistémica de AAV-PHP.eB para lograr una expresión en todo el sistema nervioso central (SNC).
RESULTADOS
Presentamos un marco para la ingeniería de sistemas CAR en los que los scFv anti-Aβ se fusionan a los dominios intracelulares de los receptores fagocíticos. Diseñamos cuatro CAR anti-Aβ independientes de FcRγ que funcionan de manera robusta en astrocitos inmortalizados y primarios, mejorando la fagocitosis y promoviendo la degradación de oligómeros de Aβ42 in vitro. Con base en estos datos, seleccionamos dos CAR para su administración in vivo a astrocitos del SNC mediante administración periférica no invasiva de AAV-PHP.eB-GFAP. Una construcción une crenezumab al dominio fagocítico de MEGF10 (Cre-Megf10), y la otra une aducanumab al dominio fagocítico de Dectin1 (Adu-Dectin1). Una sola administración de cualquiera de los CAR-A después de la formación de placas redujo significativamente la carga amiloide y la distrofia neurítica en 3 meses, mientras que la administración temprana previno la acumulación de Aβ y la patología asociada durante 2,5 meses. La secuenciación de ARN de núcleo único y la inmunotinción demostraron que ambos CARs indujeron astrocitos asociados a la enfermedad y desplazaron la microglía hacia un estado más homeostático con señales de agotamiento reducidas. Cabe destacar que los constructos divergieron parcialmente en sus efectos posteriores: Cre-Megf10 actuó principalmente sobre los estados astrocíticos, mientras que Adu-Dectin1, además, activó la microglía mediante la comunicación astrocito-microglía.
CONCLUSIÓN
Más allá del éxito de las terapias basadas en CAR en oncología, este trabajo demuestra el potencial de adaptar la tecnología CAR fagocítica al SNC. Al dirigirnos a los astrocitos, revelamos un nuevo eje terapéutico para la enfermedad de Alzheimer que complementa las funciones fagocíticas clásicamente atribuidas a la microglía y amplía el repertorio de dianas celulares para la intervención neuroinmune. La observación de que distintos diseños de CAR impulsan programas gliales parcialmente divergentes resalta la flexibilidad de esta plataforma y la oportunidad de personalizar la señalización de CAR para lograr objetivos terapéuticos específicos. De cara al futuro, la optimización continua será fundamental para maximizar la eliminación de amiloide preservando la integridad neuronal, minimizar los efectos fuera de diana y extender este enfoque a otros tipos celulares. En conjunto, estos hallazgos posicionan la ingeniería de CAR como una estrategia escalable y adaptable para el tratamiento de enfermedades neurodegenerativas.
Fuente: revista Science/ science.org