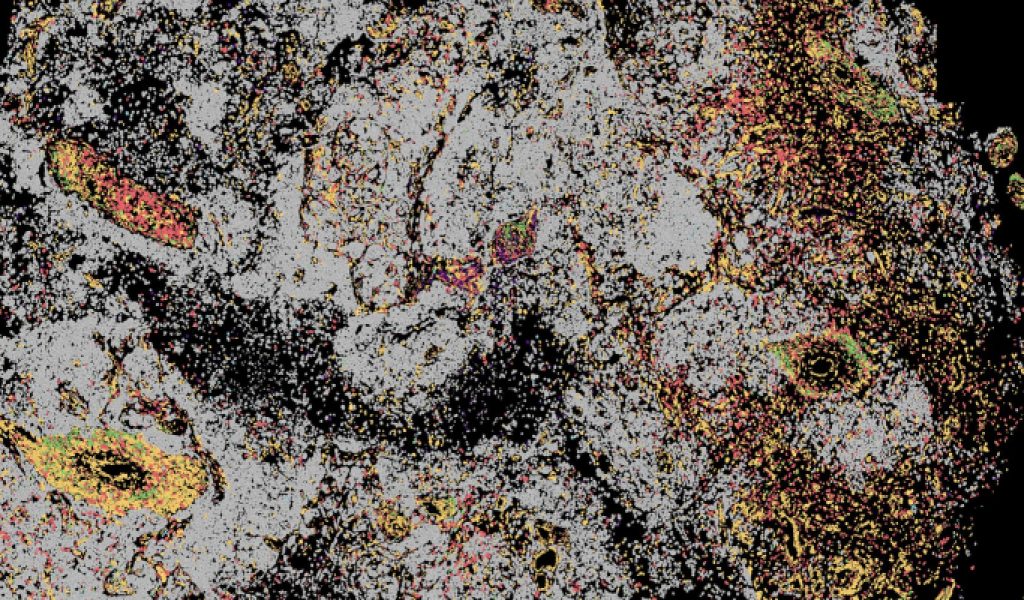- . Un nuevo estudio liderado por el Centro Nacional de Análisis Genómico (CNAG) revela cómo el líquido cefalorraquídeo contiene información clave sobre la progresión de las neoplasias del sistema nervioso central y su resistencia a los tratamientos.
- Publicada en Cell Reports Medicine , la investigación combina, por primera vez, la biopsia líquida de líquido cefalorraquídeo con un conjunto de técnicas de secuenciación de última generación.
- Estos hallazgos abren nuevas vías para el desarrollo de terapias personalizadas para pacientes con enfermedades leptomeníngeas, caracterizadas por la presencia de células cancerosas en el líquido cefalorraquídeo.
Diariamente, nuestro cerebro se baña y limpia con aproximadamente medio litro de un líquido incoloro: el líquido cefalorraquídeo. Este sistema de irrigación cerebral penetra en las capas más profundas del sistema nervioso y transporta información muy valiosa sobre lo que ocurre en su epicentro, incluida la actividad de las células inmunitarias. Hasta ahora, el líquido cefalorraquídeo se ha utilizado principalmente para diagnosticar diversas enfermedades neurológicas mediante punción lumbar, ayudando a miles de pacientes a comprender su afección.
Ahora, el Centro Nacional de Análisis Genómico (CNAG), en colaboración con la Universidad Goethe de Frankfurt (Alemania) , ha dado un paso más allá al combinar estas muestras con una serie de técnicas de secuenciación de nueva generación para descifrar el líquido cefalorraquídeo y obtener información clave sobre la evolución de los tumores cerebrales y su resistencia al tratamiento. El estudio, publicado en Cell Reports Medicine , analiza la actividad del sistema inmunitario en el líquido cefalorraquídeo, generando una imagen de alta resolución de los tipos de células inmunitarias y sus interacciones en pacientes con neoplasias del sistema nervioso central.

«Estudiar los tumores cerebrales siempre ha supuesto un gran reto, sobre todo por la dificultad de acceder a ellos», explica el Dr. Holger Heyn, autor principal del estudio, catedrático ICREA y jefe del Grupo de Genómica Unicelular del CNAG. «En este estudio, gracias al líquido cefalorraquídeo, hemos explorado el propio sistema circulatorio del cerebro y descubierto una auténtica joya oculta: información directa sobre la evolución del tumor y su interacción con el sistema inmunitario. Este hallazgo convierte al líquido cefalorraquídeo en una potente herramienta pronóstica, que nos permite descubrir biomarcadores hasta ahora desconocidos que podrían sentar las bases para el diseño de terapias más eficaces » .
Descifrando el microambiente tumoral del cerebroAunque el cerebro es un órgano inmunoprivilegiado, nuestras células inmunitarias migran hacia él para combatir los tumores. Como ocurre con cualquier enfermedad neurológica, la presencia de estas células en el líquido cefalorraquídeo aumenta significativamente en los pacientes a medida que la enfermedad progresa, con el objetivo de llegar al epicentro y combatirlo.
Los investigadores analizaron más de 70 000 células de pacientes con linfomas de líquido cefalorraquídeo, glioblastomas o metástasis cerebrales de melanoma, cáncer de mama y de pulmón, comparándolas con células de pacientes con trastornos neuroinflamatorios. El equipo de CNAG utilizó técnicas de secuenciación pioneras que permitieron estudiar individualmente el ARN de cada célula de líquido cefalorraquídeo, revelando cómo se activan los genes y cómo responden las células al tumor, incluidos los receptores de células T, que actúan como «sensores» para detectar y atacar el cáncer, y cuya expansión refleja la intensidad de la respuesta inmunitaria. El análisis se complementó con ADN tumoral para identificar posibles vulnerabilidades y transcriptómica espacial para generar un mapa detallado de las células en su entorno.
«Gracias a este enfoque innovador, hemos descubierto que cada tipo de tumor crea su propio microambiente en el líquido cefalorraquídeo, lo que refleja lo que puede estar ocurriendo en el epicentro de la enfermedad», explica el Dr. Juan Nieto, autor principal e inmunólogo del CNAG. «Esto nos ayuda a comprender mejor el comportamiento del tumor y la respuesta inmunitaria, proporcionando información muy útil para desarrollar nuevas herramientas que permitan monitorizar la dinámica tumoral».
Un paso adelante para las terapias personalizadas.Dada la agresividad de las neoplasias del sistema nervioso central y la limitada eficacia de las terapias actuales, la comunidad científica anhela comprender mejor la biología de estos tumores y los mecanismos de defensa del organismo. En esta búsqueda urgente de respuestas, este estudio representa un importante avance, al destacar nuevos biomarcadores potenciales para el diseño de terapias personalizadas más eficaces.
«Gracias a estos nuevos análisis, hemos podido identificar linfocitos T con receptores específicos capaces de reconocer células tumorales en el líquido cefalorraquídeo, cuya posible vía de entrada es a través del torrente sanguíneo», explica Paula Nieto, primera autora del estudio e investigadora del CNAG. «Esto podría permitir el diseño de terapias personalizadas, como linfocitos T modificados con receptores específicos o vacunas dirigidas, aprovechando las propias defensas del organismo para combatir el cáncer. Si bien aún queda mucho trabajo por hacer, estas estrategias podrían suponer un avance importante en el tratamiento de los tumores cerebrales, contribuyendo a terapias más precisas».
Estas inmunoterapias aprovechan las propias células T del paciente, entrenándolas o modificándolas para que reconozcan y ataquen el tumor con mayor eficacia. Entre las opciones más avanzadas se encuentran las células TCR-T (células T modificadas con receptores específicos), las células CAR-T diseñadas para detectar antígenos tumorales y las vacunas basadas en receptores, cuyo objetivo es estimular el sistema inmunitario para que actúe directamente contra el cáncer.
Actualmente, el estudio se encuentra en su segunda fase, aplicando este enfoque innovador a una cohorte ampliada de pacientes para analizar las respuestas inmunitarias antes y después del tratamiento, con el objetivo final de convertir esta nueva metodología en una herramienta analítica universal, escalable para su uso en hospitales y centros médicos de todo el mundo.
ARTÍCULO DE REFERENCIA
Nieto, Paula, et al. ‘Perfilado integrador del LCR identifica respuestas inmunitarias específicas de la enfermedad en la enfermedad leptomeníngea’. Cell Reports Medicine, marzo de 2026, pág. 102651. DOI.org (Crossref), https://doi.org/10.1016/j.xcrm.2026.102651.
Imagen: crédito foto de portada: CNAG
Fuente: Centro Nacional de Análisis Genómico/ cnag.eu